Introduzione
Le faggete del Centro Italia costituiscono ecosistemi forestali di elevata biodiversità (MARCHETTI e LOMBARDI, 2006), con una notevole ricchezza floristica e faunistica. Questi habitat sono caratterizzati dalla dominanza del faggio (Fagus sylvatica L.), ma comprendono anche numerose specie vegetali e animali che concorrono alla stabilità ecologica. Tuttavia, il cambiamento climatico e le pressioni antropiche (IPCC, 2014; RICHARDSON e PYŠEK, 2006), stanno compromettendo tali equilibri, favorendo la diffusione di organismi alloctoni e l’indebolimento della resilienza delle comunità forestali. La gestione forestale intensiva e il disboscamento possono portare alla perdita di habitat e alla diminuzione della biodiversità. La raccolta non sostenibile di legname può danneggiare la struttura del bosco. Inoltre è stato osservato come il legno morto rappresenti una componente fondamentale delle cenosi forestali. Tronchi abbattuti e marcescenti, branche e rami caduti a terra formano microhabitat molto importanti per la conservazione della biodiversità (MARCHETTI e LOMBARDI, 2006). La raccolta indiscriminata della necromassa può compromettere ed avere un impatto significativo sulle popolazioni di organismi saproxilici che vivono al loro interno. Le faggete possono essere danneggiate da inquinanti atmosferici, come il biossido di zolfo e gli ossidi di azoto, che compromettono la salute degli alberi e del suolo. L'introduzione di specie vegetali e animali non autoctone può innescare fenomeni di competizione con le specie autoctone, riducendo la biodiversità e alterando gli equilibri ecologici (RICHARDSON e PYŠEK, 2006). L'emergenza di patogeni e parassiti può creare disturbi ai popolamenti di faggio e alle altre specie associate. Per questo la salvaguardia delle faggete e della loro biodiversità è cruciale per mantenere gli equilibri ecologici e i servizi ecosistemici di cui beneficiano sia le specie naturali sia la collettività.
Il contesto ecologico delle faggete italiane
La distribuzione del faggio in Italia si estende principalmente lungo l’Appennino e le zone montane del Nord, ma alcuni boschi, come la faggeta di Monte Raschio a Oriolo Romano, si trovano a quote insolitamente basse grazie alle condizioni microclimatiche favorevoli e l’area di interesse rientra nel sito seriale transnazionale delle “Antiche faggete primordiali dei Carpazi e di altre regioni d’Europa” la cui formazione risale alla fine dell’ultima era glaciale e rappresenta un fulgido esempio di foreste non disturbate dall’antropizzazione. Tali faggete depresse, spesso vetuste e poco disturbate dall’uomo, rivestono un’importanza cruciale per la conservazione della biodiversità, in particolare per gli organismi saproxilici, ovvero quelli legati alla presenza di legno morto e in decomposizione. I coleotteri lignicoli e corticicoli rientrano tra questi.
Coleotteri lignicoli (ambrosia beetles) e corticicoli (bark beetles) e il loro ruolo ecologico
I coleotteri lignicoli hanno attirato l’attenzione negli ultimi decenni a causa delle numerose introduzioni in tutto il mondo, molte delle quali legate al commercio internazionale di materiale legnoso. In alcuni casi, sono stati osservati danni ingenti. Rappresentano un gruppo particolarmente importante di specie aliene, capaci di viaggiare inosservati all'interno di molti materiali legnosi diversi e difficili da individuare durante le ispezioni fitosanitarie (BROCKERHOFF et al., 2006). I coleotteri lignicoli delle sottofamiglie Scolytinae e Platypodinae, spesso noti come ambrosia beetles (FRANCKE GROSMANN, 1975; FACCOLI, 2021), svolgono un ruolo chiave nei processi di decomposizione del legno e nella disseminazione di funghi simbionti. Questi insetti scavano gallerie all’interno del legno ospite e trasportano spore fungine colonizzando lo xilema attraverso strutture specializzate (FRANCKE GROSMANN, 1975) chiamate micangi (Figura 1), che variano notevolmente a seconda della specie. I funghi simbionti, spesso appartenenti al genere Ambrosiella, costituiscono l’unica fonte di nutrimento per le larve.
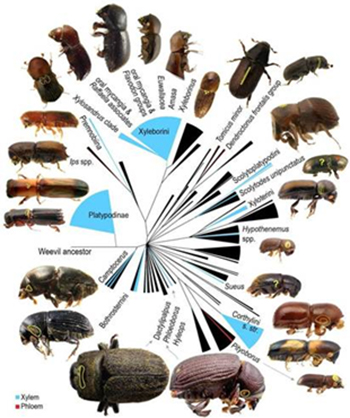
Fig. 1 Diversità del gruppo degli “ambrosia beetles”. In giallo sono evidenziati i micangi.
I corticicoli, si nutrono delle sostanze presenti nel floema della pianta ospite, raggiungono la corteccia del fusto e dei rami di alberi idonei penetrandovi attraverso un foro d’entrata. In corrispondenza di questo scavano una piazzola, detta camera nuziale o vestibolo, dove solitamente avviene l’accoppiamento.
Negli ultimi anni, numerosi focolai di infestazione da coleotteri lignicoli esotici sono stati documentati in diverse regioni italiane. Uno dei più noti riguarda un’area boschiva in provincia di Lucca, dove Xylosandrus compactus ha colonizzato una piantagione mista di carpini e querce. In Emilia-Romagna, invece, Xylosandrus germanus è stato individuato in aree periurbane su alberi ornamentali indeboliti. Nel settembre 2016, all’interno del Parco Nazionale del Circeo (Lazio, Italia) è stato rilevato il primo grande focolaio di Xylosandrus compactus e Xylosandrus crassiusculus in un ecosistema naturale europeo (VANNINI et al., 2017). Le tre specie di Xylosandrus occupano nicchie ecologiche diverse, infestando rami di vario diametro, il che amplifica il rischio di compromissione dell'intera struttura forestale.
X. compactus predilige, generalmente, rami più sottili, inferiori ai 2–3 cm di diametro, mentre X. germanus e X. crassiusculus scavano gallerie in tronchi più spessi, oltre i 2 cm di diametro. La presenza di questi scolitidi nelle faggete potrebbe dunque aggravare il deperimento degli alberi, già esposti a stress ambientali legati ai cambiamenti climatici (CONTARINI et al., 2020). Gli alberi attaccati presentano danni quali disseccamento, deperimento dei rami e rottura dei germogli. Questi casi sottolineano l’ampia plasticità ecologica di queste specie, capaci di adattarsi a condizioni ambientali e tipologie arboree differenti. L’assenza di nemici naturali e la capacità di riprodursi partenogeneticamente ne amplificano il potenziale invasivo.
Materiali e metodi
Il sito di studio si trova all’interno del Parco Naturale Regionale di Bracciano-Martignano e risulta di particolare interesse naturalistico. Si trova in un’area localizzata a 42°09'43.5"N 12°09'15.7"E di coordinate. L’area presenta una morfologia tipica, la natura vulcanica e le caratteristiche climatiche ne influenzano fortemente gli aspetti vegetazionali, determinando l’elevata diversità tipologica dei boschi. La cinta collinare che circonda i laghi di Bracciano e Martignano in poche centinaia di metri di dislivello (da 160 a 610 m s.l.m.), ospita una successione vegetazionale che può definirsi completa in quanto partendo alle quote più basse dalla macchia mediterranea si arriva fino alle faggete, passando attraverso querceti termofili di roverella (Quercus pubescens L.), cerrete e castagneti. All’interno di questo Parco, troviamo un’Area Protetta, la Faggeta vetusta depressa di Monte Raschio nel comune di Oriolo Romano (VT), Patrimonio dell' Umanità UNESCO e area ZSC IT6010034, con un’estensione di 74 ha (Figura 2).
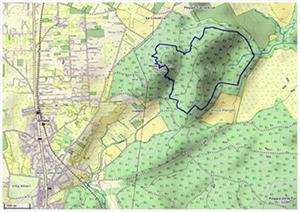
Fig. 2 ZSC IT6010034, Faggeta vetusta di Monte Raschio.
Le attività di campo si sono svolte tra febbraio e ottobre 2024. Sono state impiegate trappole multifunnel innescate con etanolo, attrattivo particolarmente efficace (RANGER et al., 2012) per gli ambrosia beetles (FRANCKE GROSMANN, 1975; FACCOLI, 2021). Le trappole sono state appese a circa due metri da terra e i campioni raccolti ogni 15 giorni (Figura 3). Sono costituite da una serie di 12 imbuti neri, di circa 20 cm di diametro, posizionati verticalmente e hanno alla base un cilindro di raccolta del campione dotato di retina basale, per permettere la fuoriuscita di acqua piovana. L’attrattivo è stato sostituito ogni due settimane per tutta la durata del monitoraggio, contestualmente alla raccolta dei campioni, avvenuta con la stessa frequenza. In totale sono state posizionate nove trappole. L’area è stata suddivisa in tre blocchi, in ognuno dei quali sono state collocate tre trappole secondo uno schema triangolare, posizionate l’una dall’altra a 70-80 m. Le analisi di laboratorio hanno incluso l’identificazione morfologica e il conteggio degli individui catturati.

Fig. 3 Posizione delle trappole multifunnel nella faggeta vetusta di Oriolo Romano (VT). (Foto I. Fusco)
Tecniche di identificazione e diagnosi
L’identificazione dei coleotteri lignicoli e corticicoli avviene prevalentemente per via morfologica, osservando caratteri diagnostici come forma del pronoto, dimensioni del rostro, struttura delle elitre, peluria e quindi attraverso l’uso di chiavi dicotomiche specifiche con l’utilizzo di uno stereomicroscopio. Tuttavia, in contesti critici o per stadi giovanili è possibile ricorrere a tecniche molecolari basate su DNA barcoding, che permettono di distinguere specie morfologicamente simili. Altri strumenti utili sono le trappole selettive con attrattivi volatili, che permettono anche un monitoraggio quantitativo stagionale.
Al termine di ciascun periodo di campionamento, i contenitori di raccolta sono stati svuotati all’interno di barattoli a chiusura ermetica (Fig. 4). Il materiale così raccolto è stato quindi portato nel laboratorio di “Strategie Innovative per il Monitoraggio degli insetti” del Dipartimento DAFNE, dell’Università degli Studi della Tuscia (VT), per la fase di svuotamento e pulizia delle catture effettuate.
Con l’ausilio di pinzette o pennelli è stato possibile capire le caratteristiche morfologiche, censendo tutti gli scolitidi dagli insetti non-target; si è poi proceduto all’identificazione e alla conta degli esemplari suddividendoli nelle diverse specie.

Fig. 4 Provetta per il campionamento.
Risultati
I risultati dell’attività di monitoraggio hanno portato alla cattura di numerosi individui, appartenenti a specie autoctone e alloctone. La tabella riassume i dati delle catture, mostrando il numero di individui per ogni specie trovata e la loro percentuale rispetto al totale (Tabella 1).

Tab. 1 Specie di ambrosia e bark beetles, numero di individui catturati e percentuale sul totale. In rosso le specie considerate alloctone per l’Italia.
Sono state identificate 13 specie di coleotteri lignicoli. Dai risultati ottenuti tramite analisi statistica e con l’applicazione del “software r”, tra le più abbondanti si segnalano Xylosandrus germanus, con picchi di volo tra maggio e luglio, e Xyleborinus saxesenii, presente in tutto il periodo e mostrano un numero di catture statisticamente maggiore rispetto alle altre specie (p<0,05) (Figura 5). Anisandrus dispar ha mostrato una distribuzione irregolare ma significativa. La presenza di Taphrochychus bicolor è risultata correlata al deperimento degli alberi, probabilmente associata a siccità prolungata.
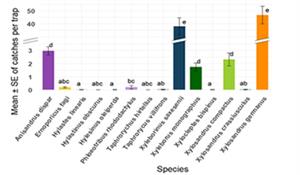
Fig. 5 Numero medio di catture per trappola per le diverse specie. Lettere diverse indicano una differenza statisticamente significativa (p<0,05).
Successivamente i dati raccolti sono stati organizzati in curve di volo stagionali che evidenziano l’attività specifica di ciascuna specie (Figura 6). Il grafico permette di osservare se esiste una relazione tra l'attività di volo delle specie e le variazioni della temperatura, mostrando i periodi in cui ogni specie è più attiva. Si nota che per Xylosandrus germanus e Xyleborinus saxesenii si registrano due picchi in due fasce temporali distinte. La prima da marzo a maggio e la seconda da maggio a luglio, con particolare riferimento al giorno 6 giugno 2024. Le due specie hanno un’elevata presenza in estate, quando la temperatura è più alta. Anche per X. compactus si possono notare due picchi negli stessi periodi, anche se con numeri decisamente più bassi. Da luglio in poi si osserva un appiattimento delle curve di volo di tutte le specie.
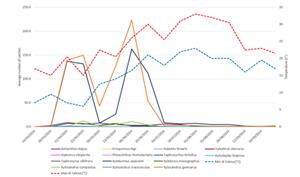
Fig. 6 Andamento degli eventi di volo delle specie catturate durante la stagione di monitoraggio. Le linee tratteggiate indicano la temperatura minima e massima nel sito.
Dinamiche ecologiche e interazioni trofiche
I coleotteri lignicoli non agiscono isolatamente nell’ecosistema forestale, ma sono inseriti in una rete complessa di interazioni trofiche e simbiotiche. La loro attività di scavo crea microhabitat che vengono colonizzati da acari, nematodi e funghi secondari, contribuendo alla formazione di nicchie ecologiche. Inoltre, le larve di alcune specie di ditteri e imenotteri parassitoidi si sviluppano nelle gallerie, alimentandosi dei coleotteri o dei loro simbionti. Questo processo amplifica la biodiversità complessiva e rende i coleotteri un tassello fondamentale nel funzionamento della faggeta. Le modifiche causate dalle specie aliene, che spesso non hanno antagonisti naturali nei nuovi ambienti, possono quindi innescare squilibri a cascata.
Discussione
I risultati suggeriscono che la presenza e l’espansione delle specie aliene invasive siano strettamente legate a condizioni climatiche stressanti. L’aumento delle temperature e la siccità favoriscono la comparsa di segnali chimici (etanolo) che attraggono gli ambrosia beetles (RANGER et al., 2012; FRANCKE GROSMANN, 1975; FACCOLI, 2021). Il legame tra insetti, piante ospiti e simbionti fungini si rivela fondamentale per comprendere le dinamiche ecologiche in atto. Xylosandrus germanus, in particolare, si dimostra una minaccia concreta per le faggete, per la sua capacità di colonizzare alberi vivi e per la trasmissione di funghi potenzialmente patogeni (HARRINGTON, 2005).
Confronto con faggete di altri paesi europei
Le faggete del Centro Italia, per quanto uniche per la loro altitudine e composizione floristica, presentano dinamiche simili a quelle osservate in faggete di altri paesi europei, come la Germania, l’Austria e la Slovenia. Studi condotti nelle foreste della Turingia (Germania centrale) hanno evidenziato come Xylosandrus germanus e Xyleborinus saxesenii mostrino strategie ecologiche convergenti, colonizzando tronchi di latifoglie morti o morenti (BROCKERHOFF et al., 2006). La differenza principale risiede nella pressione climatica: le faggete italiane stanno affrontando temperature più elevate e periodi siccitosi più lunghi, che accelerano i fenomeni di deperimento e favoriscono l’espansione delle specie invasive. Il confronto internazionale può quindi offrire spunti utili per strategie di adattamento climatico basate su modelli condivisi.
Normative e gestione forestale
Le politiche europee e italiane riconoscono la necessità di conservare le faggete vetuste. La Direttiva Habitat (92/43/CEE) include tali ecosistemi tra gli habitat prioritari e ne promuove la gestione sostenibile attraverso la “Rete Natura 2000”. Tuttavia, la gestione operativa richiede strumenti flessibili che integrino monitoraggi fitosanitari, lotta biologica e controllo del materiale forestale in transito. L’uso di trappole a feromoni e l’adozione di protocolli di quarantena rappresentano strumenti utili, ma è fondamentale anche formare operatori forestali, tecnici e cittadini per riconoscere precocemente le infestazioni da coleotteri esotici invasivi.
Prospettive future e raccomandazioni
Per affrontare le sfide legate alla gestione delle specie lignicole alloctone, è necessario promuovere un approccio integrato basato su: (1) monitoraggi continuativi e multistagionali; (2) collaborazione tra enti gestori, ricercatori e operatori del territorio; (3) adozione di tecnologie digitali per la raccolta e l’analisi dei dati (es. GIS, app di “citizen science”). Inoltre, investire nella ricerca sulla biologia riproduttiva e sulla tolleranza ecologica delle specie aliene permetterà di prevedere la loro espansione. Le faggete italiane possono diventare laboratori a cielo aperto per sperimentare modelli di conservazione replicabili anche in altri ecosistemi forestali.
Conclusioni
I dati raccolti mostrano con chiarezza come i cambiamenti climatici e la globalizzazione dei commerci stiano contribuendo all’introduzione e alla diffusione di coleotteri lignicoli esotici in ambienti forestali italiani (BROCKERHOFF & LIEBHOLD, 2017). La prevenzione e il contenimento richiedono approcci multidisciplinari che integrino ecologia, genetica, tecnologia e governance del territorio. La gestione sostenibile delle faggete italiane non può prescindere dal monitoraggio fitosanitario e dalla consapevolezza dei rischi legati alle specie invasive. Solo attraverso un’azione concertata sarà possibile tutelare la biodiversità forestale e garantire la resilienza degli ecosistemi.
Ringraziamenti: Desidero esprimere la mia più sincera gratitudine al Prof. Mario Contarini per la disponibilità, la guida attenta e il costante supporto scientifico e umano che ha reso possibile la realizzazione di questo lavoro. La sua competenza e la sua passione per la ricerca sono state per me fonte di grande ispirazione.
Un sentito ringraziamento va anche al Laboratorio di Strategie Innovative per il Monitoraggio degli Insetti del Dipartimento DAFNE dell’Università degli Studi della Tuscia (Viterbo), per avermi accolto e offerto l'opportunità di svolgere attività di ricerca in un contesto stimolante e altamente formativo.
Bibliografia
-BROCKERHOFF, E.G., CARNUS, J.M., PARROTTA, J., ARBEZ, M., JACTEL, H., KREMER, A., LAMB, D., 2006 - Planted Forests and Biodiversity. Journal of Forestry, 65-77.
-BROCKERHOFF, E.G., LIEBHOLD, A.M., 2017 - Ecology of forest insect invasions. Forest invasion. Volume 19, 3141-3159.
-CONTARINI, M., VANNINI, A., GIARRUZZO, F., FACCOLI, M., MORALES-RODRIGUEZ, C., ROSSINI, L., SPERANZA, S., 2020 - First record of Xylosandrus germanus (Blandford) (Coleoptera: Curculionidae, Scolytinae) in the Mediterranean scrubland in Southern Italy, and its co-presence with the co-generic species X. compactus (Eichhoff) and X. crassiusculus (Motschulsky). Bulletin OEPP/EPPO, 50 (2), 311–315.
-FACCOLI, M., 2021- Xylosandrus compactus, un nuovo parassita forestale invade l’Italia. Forest@ Rivista di Selvicoltura ed Ecologia Forestale, pp. 8-14.
-FRANCKE GROSMANN, H., 1975 - Epizoic and Endozoic Transmission of the Fungal Symbionts by the Ambrosia Beetle Xyleborus saxeseni (Coleoptera: Scolytidae). Entomologia Generalis, 279 - 292.
-HARRINGTON, C.T., 2005 - Ecology and evolution of mycophagous bark beetles and their fungal partners. Ecological and Evolutionary Advances in Insect-Fungal Associations, Oxford University Press, Oxford, 257-291.
-IPCC., 2014. AR5 Synthesis Report.
-MARCHETTI, M., LOMBARDI, F., 2006 - Analisi quali-quantitativa del legno morto in soprassuoli non gestiti: il caso di "Bosco Pennataro", Alto Molise. L’Italia Forestale e Montana, 224, 3–11.
-RANGER, C.M., REDING, M. E., SCHULTZ, P.B., OLIVER, J. B., 2012 - Influence of flood-stress on ambrosia beetle host-selection and implications for their management in a changing climate. Agricultural and Forest Entomology, 14, 27–34.
-RICHARDSON, D.M., PYŠEK, P., 2016 - Plant invasions: merging the concepts of species invasiveness and community invasibility. Progress in Physical Geography. Progress in Physical Geography Earth and Environment 30(3):409-431.
-VANNINI, A., CONTARINI, M., FACCOLI, M., DALLA VALLE, M., RODRIGUEZ, C. M., MAZZETTO, T., GUARNERI, D., VETTRAINO, A. M., SPERANZA, S., 2017 - First report of the ambrosia beetle Xylosandrus compactus and associated fungi in the Mediterranean maquis in Italy, and new host–pest associations. The likely impact of climate change on the biodiversity of Italian forests. Bulletin OEPP/EPPO, 47 (1), 100–103.
Testi di riferimento indicati dall’autore
-AREND, J.P., EISENBARTH, E., PETERCORD, R., 2006 - Buchenkomplexkrankheit in Luxemburg und Rheinland-Pfalz – Schadsymptome, Ausmaß und Entwicklung der Schäden. Mitteilungen aus der Forschungsanstalt für Waldökologie und Forstwirtschaft Rheinland-Pfalz 11–22.
-BARDGETT, R.D., VAN DER PUTTEN, W.H., 2014 - Belowground biodiversity and ecosystem functioning. Nature, 515, 505–511.
-CLAUSER, F., 2003 - Per una sociologia forestalOe dell’ordine spontaneo. L’Italia Forestale e Montana, 58 (2): 134-142.
-GUARNERI, D., VETTRAINO, A. M., SPERANZA, S., 2017 - First report of the ambrosia beetle Xylosandrus compactus and associated fungi in the Mediterranean maquis in Italy, and new host–pest associations. The likely impact of climate change on the biodiversity of Italian forests. Bulletin OEPP/EPPO, 47 (1), 100–103.
-LEGAMBIENTE., 2024. Biodiversità a rischio 2024.
-O’HARA, K., WALTERS, B., 2006 - Planted Forests and Biodiversity, 65–77.
-ROQUES, A., KENIS, M., LEES, D., LOPEZ-VAAMONDE, C., RABITSCH, W., RASPLUS, D. J. Y., ROY, B., 2010 - Alien Terrestrial Arthropods of Europe. BIORISK - Biodiversity and Ecosystem Risk Assessment, 4, 1028.