Introduzione: Il “Piano Nazionale di emergenza per alimenti e mangimi” Il “Piano nazionale di emergenza per alimenti e mangimi” (adottato con l’atto di Intesa Stato- Regioni del 10 maggio 2023) prevede, nello specifico dell’Allegato 1, par. 3, l’interazione con il “Piano per eventi con armi o agenti di tipo chimico, biologico, radiologico e nucleare”, nel caso di situazioni di emergenza in cui sia stato individuato un pericolo biologico; in particolare, tra le situazioni che richiedono l’attivazione della preposta Unità di Crisi, sono previsti “sospetti o indicazioni di terrorismo biologico”. L’esplicito riferimento al concetto di terrorismo biologico (o bioterrorismo) rimarca in tale contesto la correlazione tra la specifica categoria di pericolo e il consumo di alimenti.
Bioterrorismo e armi biologiche Ogni atto che abbia un effetto di natura terroristica può essere definito come terrorismo, ma è meglio ricorrere alla definizione più precisa di «condotta terroristica» presente nel Codice Penale (art. 270-sexies «Condotte con finalità di terrorismo»), che cita: «Sono considerate con finalità di terrorismo le condotte che, per la loro natura o contesto, possono arrecare grave danno ad un Paese o ad un'organizzazione internazionale e sono compiute allo scopo di intimidire la popolazione o costringere i poteri pubblici o un'organizzazione internazionale a compiere o astenersi dal compiere un qualsiasi atto, o destabilizzare o distruggere le strutture politiche fondamentali, costituzionali, economiche e sociali di un Paese o di un'organizzazione internazionale». Il terrorismo costituisce, nella sostanza, una forma di guerra, condotta in maniera asimmetrica, tra due o più nemici, che non rispondono alle medesime regole.
Per quanto premesso, il bioterrorismo può essere definito «utilizzo intenzionale di agenti biologici (1) (virus, batteri o tossine) in azioni contro l'incolumità pubblica (attentati, sabotaggi, stragi o minacce), al fine di creare panico e isteria collettiva». Una definizione normativa degli agenti biologici è fornita dal D. Lgs. 9 aprile 2008, n. 81 (2), che ne propone, successivamente, una ripartizione in quattro gruppi (3), a rischio individuale/collettivo crescente (4), in relazione ai criteri di infettività, di patogenicità, di trasmissibilità e spettro d’ospite, nonché di neutralizzabilità (5); tuttavia, la migliore classificazione degli agenti biologici intesi quali arma da guerra è quella dei Centers for Disease Control and Prevention - CDC (sede principale ad Atlanta-USA), che li suddivide nelle tre categorie (6) «A» 8 (7), «B» (8) e «C» (9), in funzione dei seguenti quattro criteri:
- l’impatto sulla salute pubblica e il tasso di mortalità;
- la facilità di disseminazione e di trasmissione tra individui;
- la capacità di causare panico e disgregazione sociale;
- il livello di preparazione e di azioni necessarie per la difesa della salute pubblica.
I CDC identificano ulteriori biotossine potenzialmente utilizzabili per scopi terroristici, tra le quali si ricordano, in particolare, la brevetossina, la saxitossina, la tetrodotossina (afferenti alla famiglia delle biotossine marine) e i tricoteceni (micotossine).
L’arma biologica prevede la contemporanea presenza di due elementi costitutivi essenziali: uno o più agenti biologici utilizzati al fine di uccidere/debilitare/rendere inoffensivo il nemico e un mezzo di diffusione, che renda l’agente biologico diffusivo. La Commissione delle Nazioni Unite per gli armamenti classici con la Risoluzione del 12 agosto 1948 colloca le armi biologiche tra le armi di distruzione di massa (WMD), in quanto in grado di determinare un numero elevato di vittime con un impiego limitato di risorse.
Nonostante il termine bioterrorismo costituisca un neologismo degli anni ‘90 del secolo scorso, la guerra biologica e l’impiego delle armi biologiche sono fenomeni documentati fin dalle epoche più antiche, proprio in ragione della loro premessa capacità di colpire numerosi individui pressoché simultaneamente. La sottostante Tabella 1 riporta alcuni degli episodi storici più noti in cui hanno trovato impiego armi biologiche, tra cui si ricordano, in particolare:
- l’assedio di Caffa (1346), durante il quale i tartari, per espugnare la città sotto controllo genovese, catapultarono i cadaveri dei loro compagni appestati all’interno delle mura (10);
- l’inganno perpetrato dal conquistador Francisco Pizarro, che donò agli Inca il vestiario dei guerrieri spagnoli colpiti, probabilmente, da infezione vaiolosa, contribuendo in maniera determinante alla capitolazione (1531) dei nativi e del loro millenario Impero;
- la consegna di buste/pacchi postali indirizzati ad alcuni uffici giornalistici e a due senatori del Partito Democratico negli USA (11), pochi giorni dopo l’attentato alle Twin Towers di New York (11 settembre 2001).
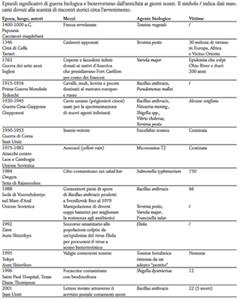
Tabella 1: Episodi di impiego di armi biologiche (Fonte: Emergency Care Journal, 2007).
Le caratteristiche essenziali per identificare e valutare l’impatto delle armi biologiche sono:
- la modalità di trasmissione (penetrazione respiratoria/inalatoria, digerente, cutanea, per iniezione/ inoculazione);
- il periodo di incubazione (solo per i microrganismi), caratterizzato da estrema variabilità, pertanto, il parametro che maggiormente incide sulla scelta di impiego tattico o strategico dell’aggressivo;
- la modalità di disseminazione intenzionale nell’ambiente (aerosol, contaminazione diretta di cibo ed acqua, vettori (12) e individui contagiosi);
- il potere patogeno;
- l’indice di letalità (13);
- la carica o dose infettante (solo per i microrganismi);
- la persistenza nell’ambiente;
- il quadro clinico e la sintomatologia.
Uno specifico approfondimento meritano le tossine (14), in particolare per quanto concerne quelle di origine batterica (15), distinguibili tra:
- endotossine, costituenti della parete cellulare, di natura lipopolisaccaridica, termostabili e non neutralizzabili da anticorpi;
- esotossine, sintetizzate in situazioni sfavorevoli, di natura proteica, termolabili, neutralizzabili da anticorpi, con rapida insorgenza dei sintomi (1 - 12 ore).
Caratteristiche peculiari delle tossine sono:
- il periodo di latenza, che intercorre tra la penetrazione della tossina e la comparsa dei sintomi;
- l’indice di letalità e la dose letale media (c.d. DL50 - vedasi Tabella 2) (16).
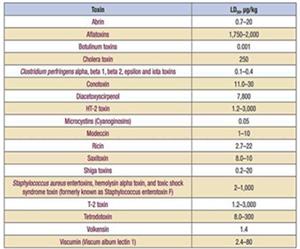
Tabella 2: DL50 di alcune biotossine (Fonte: Australia Group, 2018).
In funzione delle caratteristiche specifiche per ciascun agente biologico, il relativo utilizzo può essere finalizzato al conseguimento di obiettivi:
- bellici/terroristici, in quanto l’agente si presenta di difficile individuazione per la normale strumentazione campale disponibile e sviluppa una manifestazione differita della sintomatologia;
- strategici o tattici: i primi prevedono l’impiego di agenti biologici facilmente trasmissibili, dispersi su substrati condivisi, quali aria e/o acqua, lunghi tempi di incubazione, riscontro a lungo termine, coinvolgimento di aree estese e di un alto numero di individui; i secondi (17) di agenti non contagiosi, disseminati su substrati specifici, brevi periodi di incubazione/latenza, ridotta persistenza, azione immediata e limitata nell’estensione;
- diretti (morte o inabilitazione del personale) o indiretti (riduzione delle risorse alimentari ed economiche, nonché delle dotazioni di mezzi/materiali di importanza strategica/tattica; impatto sul morale del personale).
 Tabella 3: Vantaggi e svantaggi derivanti dall’impiego operativo delle armi biologiche.
Tabella 3: Vantaggi e svantaggi derivanti dall’impiego operativo delle armi biologiche.
La Tabella 3 riassume schematicamente i vantaggi e gli svantaggi derivanti dall’impiego operativo delle armi biologiche.
Per i c.d. nuovi agenti (18), qualora normalmente innocui allo stato naturale, le caratteristiche sulle quali operare per trasformarli in aggressivi biologici per la specifica finalità considerano:
- la farmaco-resistenza;
- l’insensibilità ai vaccini tradizionali e ai normali fattori immunologici;
- l’aumento della persistenza nell’ambiente;
- l’aumento della resistenza nei confronti delle sostanze disinfettanti/bonificanti;
- la produzione in grandi quantità di tossine conosciute o di nuova sintesi;
- la specificità del potere patogeno (colpire esclusivamente una determinata razza all’interno di una popolazione di individui appartenenti alla stessa specie).
Le Convenzioni internazionali essenziali in materia di armi biologiche sono:
- il “Protocollo di Ginevra” (1925), che riguarda la proibizione dell’impiego dei metodi di guerra biologica, pur ammettendone l’utilizzo per ritorsione; costituisce una norma di Diritto Consuetudinario Internazionale;
- la “Convenzione per le armi biologiche” (BCA), firmata a Washington il 10 aprile 1972, inerente al divieto di progettare, immagazzinare e utilizzare armi biologiche o a base di tossine, nonché sull’obbligo della distruzione di quelle possedute; i suoi principali problemi attuativi riguardano la detenzione di armi biologiche per finalità di ricerca e profilassi, la mancanza di verifiche imparziali e le ispezioni sottoposte al diritto di veto del Consiglio di Sicurezza dell’ONU;
- “The Australia Group”, forum informale di Paesi che, attraverso l’armonizzazione dei controlli sulle esportazioni, mira a garantire che tali attività non contribuiscano allo sviluppo delle armi chimiche e biologiche, sostenendo gli obiettivi della BWC; la sua funzione è quella di ostacolare la produzione di armi chimiche e biologiche, senza impedire il normale commercio di materiali e attrezzature utilizzate per scopi legittimi.; oggi è costituito da 41 membri, tra i quali tutti gli Stati aderenti alla BWC e tutti quelli costituenti la UE.
L’Unione Europea ha elaborato tre specifici atti in materia di lotta al bioterrorismo:
1. la Comunicazione della Commissione del 2 giugno 2003 “predisposizione e reazione agli attentati biologici e chimici (sicurezza sanitaria)”;
2. la Comunicazione della Commissione del 28 novembre 2005 “potenziamento del coordinamento della programmazione generale della preparazione alle emergenze sanitarie a livello dell’Unione europea”;
3. il Libro verde della Commissione dell’11 luglio 2007, “sulla preparazione contro gli attacchi biologici”.
La Comunicazione della Commissione del 2 giugno 2003, in particolare, prevede, nell’ambito della prevenzione degli atti terroristici e della reazione alle loro conseguenze, una mobilitazione di operatori e risorse nel settore della sicurezza dei prodotti alimentari, pur ritenendo che l’Unione disponga “di un ampio dispositivo legislativo (19), che copre la produzione primaria di prodotti agricoli e la produzione industriale di preparati alimentari” e, di conseguenza, “non è necessario porre in essere nuovi sistemi, ma è piuttosto opportuno adeguare i meccanismi attuali al fine di migliorare il loro funzionamento tenendo conto della minaccia bioterroristica”. Pertanto, la UE, reputando il metodo HACCP (art. 5 del Reg. CE n. 852/2004) adeguato per l’efficiente gestione dello specifico pericolo, ha “congelato” l’evoluzione della materia alla data del 9 gennaio 2008; di contro, gli USA hanno legalmente adottato il sistema HARPC (20), a partire dall’anno 2015, quale nuova metodica di gestione della sicurezza delle filiere alimentari.
Agenti biologici potenzialmente impiegabili per atti di bioterrorismo alimentare
Ripercorrendo l’excursus storico in Tabella 1, si possono evidenziare l’episodio del 1984 in Oregon (USA), che ha visto la morte di 750 individui che avevano consumato cibo contaminato intenzionalmente con Salmonella tiphymurium e poi somministrato “in salad” nei bar e ristoranti, e quello del 1996 presso il Saint Paul Hospital in Texas (USA), con il decesso di 12 persone ospedalizzate che avevano consumato focaccine contaminate con una brodocultura di Shigella dysenteriae; in entrambi i casi l’agente utilizzato a scopo bioterroristico è rappresentato da un batterio tipicamente responsabile di Malattia Trasmissibile con gli Alimenti (MTA).
In relazione alla citata classificazione degli agenti biologici impiegati quale arma da guerra predisposta dai CDC americani, possiamo individuare, per il potenziale impiego quali strumento per perpetrare atti di bioterrorismo alimentare, i seguenti microrganismi/tossine, responsabili di classiche forme di MTA, a seguito della loro ingestione con alimenti e/o acqua contaminati:
- categoria “A”:
• tossina botulinica (21) sintetizzata da Clostridium botulinum, responsabile di una tipica forma di intossicazione alimentare, definita botulismo; la via di trasmissione è per ingestione della tossina preformata presente nella matrice alimentare; la sintomatologia è di tipo neurologico (paralisi flaccida simmetrica discendente), con comparsa dei sintomi 12-36 ore dall’ingestione; il tasso di letalità, in assenza di trattamento con siero antibotulinico, può arrivare al 70-80%; l’impiego della tossina a scopo terroristico presenta i vantaggi della facilità di produzione e dell’elevata letalità, ma i contestuali svantaggi di essere facilmente inattivata con il calore (85°C per 5 minuti), l’esistenza dell’antitossina e l’elevata difficoltà operativa di contaminazione di alimenti/acqua: nel complesso si può affermare che l’impatto dell’azione sarebbe relativo sulla popolazione, in quanto sia limitato ai soli soggetti che consumano la porzione di prodotto contaminata, sia perché essenzialmente interessati i soli prodotti c.d. ready to eat (RTE) (22);
- categoria “B”:
• Brucella melitensis, per consumo di carni e prodotti a base di carne poco cotti o crudi, nonché di prodotti lattiero-caseari non pastorizzati; non esiste un vaccino e il tasso di letalità è del 2-5%; è malattia zoonotica e la trasmissione umana avviene per contatto diretto; non esiste evidenza di un suo precedente utilizzo in atti di bioterrorismo (vds. Tabella 4);
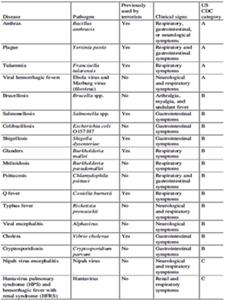
Tabella 4: Agenti biologici: precedenti impieghi di natura terroristica (Fonte: Biological Toxins and Bioterrorism, 2015).
• tossina epsilon (ETX) del Clostridium perfringens, responsabile di una tipica forma di tossinfezione alimentare, per consumo di carni e prodotti a base di carne poco cotti o crudi, nonché di prodotti lattiero-caseari non pastorizzati; la tossina agisce sulla permeabilità della membrana eritrocitaria (effetto emolitico) e presenta notevoli similitudini strutturali con l’aerolisina, prodotta da Aeromonas spp.; non esiste un vaccino e il tasso di letalità è del 15-25% (23); è malattia zoonotica, ma priva di trasmissione umana;
• Salmonella enterica, responsabile di una tipica forma di infezione alimentare, per consumo di alimenti e acqua contaminati; il tasso di letalità è del 12-30%, nonostante l’esistenza di uno specifico vaccino; non è malattia zoonotica, ma la trasmissione umana avviene per contatto diretto; il batterio è stato precedentemente utilizzato in atti di bioterrorismo (vds. Tabella 4);
• E. coli produttori di tossina Shiga-like (STEC, VTEC, EHEC), responsabile di una tipica forma di tossinfezione alimentare, per consumo di alimenti (24) e acqua contaminati; il batterio è responsabile di forme di enterocolite emorragica e della c.d. sindrome emolitico-uremica (SEU), soprattutto negli individui anziani e giovani, rispettivamente, mentre normalmente nell’adulto determinano forme lievi o asintomatiche; è malattia zoonotica (presente uno specifico vaccino) e la trasmissione umana avviene per contatto diretto; non esiste evidenza di un suo precedente utilizzo in atti di bioterrorismo (vds. Tabella 4);
• Shigella dysenteriae, responsabile di una tipica forma di tossinfezione alimentare (25), per consumo di alimenti e acqua contaminati; non esiste un vaccino e il tasso di letalità è del 1-20%, non è malattia zoonotica, ma la trasmissione umana avviene per contatto diretto; il batterio è stato precedentemente utilizzato in atti di bioterrorismo (vds. Tabella 4);
• l’enterotossina B sintetizzata da Staphylococcus aureus, responsabile di una tipica forma di intossicazione alimentare, per consumo di alimenti contaminati; la tossina, di natura proteica e caratterizzata dalla termostabilità, agisce a livello gastroenterico, determinando vomito e diarrea, fino a casi estremi di shock ipovolemico (26); non esiste una antitossina specifica;
• Vibrio cholerae, responsabile di una tipica forma di intossicazione alimentare, per consumo di alimenti e acqua contaminati; la tossina colerica agisce sulle cellule epiteliali dell’intestino tenue, promuovendo la secrezione di cloruri e determinando, per richiamo osmotico, un afflusso passivo di liquidi, da cui la comparsa di diarrea acquosa (c.d. ad acqua di riso), con scariche brevi e frequenti, che possono portare a morte per disidratazione e shock ipovolemico (27); il tasso di letalità è del 50-60%, nonostante l’esistenza di uno specifico vaccino; non è malattia zoonotica e non avviene la trasmissione umana; la tossina è stata precedentemente utilizzata in atti di bioterrorismo (vds. Tabella 4);
• Cryptosporidium parvum, protozoo (unicellulare, eterotrofo) considerato un parassita dell’acqua; nell’uomo la malattia è conosciuta con il nome di criptosporidiosi e si contrae ingerendo le oocisti (28) presenti in acqua e/o alimenti (prodotti ortofrutticoli) contaminati; non esiste evidenza di un suo precedente utilizzo in atti di bioterrorismo (vds. Tabella 4);
- categoria “C”:
• l’infezione da virus Nipah è una zoonosi emergente che si trasmette all’uomo attraverso contatto diretto con animali infetti o ingerendo cibo dagli stessi contaminato; i pipistrelli della frutta e le volpi volanti (genere Pteropus) sono gli ospiti naturali del virus; può essere trasmesso tra esseri umani attraverso lo stretto contatto con un individuo infetto; la presentazione clinica varia da una infezione asintomatica a una forma respiratoria acuta (polmonite atipica), fino all’encefalite fatale, con comparsa di convulsioni e coma entro 24-48 ore; il tasso di letalità è stimato tra il 40 e il 75% dei soggetti infettati; non esiste evidenza di un suo precedente utilizzo in atti di bioterrorismo (vds. Tabella 4).
Tra le tossine identificate dai CDC quali ulteriori agenti biologici potenzialmente utilizzabili per scopi terroristici, le seguenti biotossine marine (vds. Tabella 5) e micotossine:
- brevetossine (BTXs), liposolubili e termostabili, prodotte dalla dinoficea Karenia brevis; il loro meccanismo d’azione determina l’inibizione della trasmissione neuromuscolare nei muscoli scheletrici, causando la sintomatologia neurologica e gastrointestinale dell’intossicazione nota come Neurological Shellfish Poisoning (NSP) (29);

Tabella 5: Biotossine marine (Fonte: Marine and Freshwater Toxins, 2016).
- saxitossine (STXs), idrosolubili e termostabili, attualmente se ne conoscono oltre 30 analoghe, prodotti dalle dinoficee Alexandrium spp. e Gymnodinium catenatum, la cui combinazione può determinare la sindrome Paralytic Shellfish Poisoning (PSP); la tossicità è esclusivamente di tipo acuto e il loro meccanismo d’azione si estrinseca causando l’arresto della trasmissione dell’impulso nervoso nei nervi periferici e nelle fibre muscolari scheletriche, con la comparsa, nei casi più gravi, di paralisi, difficoltà nell’atto respiratorio e sensazione di soffocamento;
- tetrodotossina (TTX), rappresenta una delle più potenti tossine non proteiche, ampiamente distribuita nel mondo animale acquatico marino (soprattutto pesci della famiglia Tetraodontidae, tra cui 80 specie del c.d. pesce palla (30)); il meccanismo d’azione si estrinseca sui canali del sodio, determinando il blocco della conduzione dell’impulso lungo i nervi sensitivi e motori e, nei casi più gravi, l’insorgenza di una grave insufficienza respiratoria, aritmia cardiaca e morte;
- tricoteceni, che annoverano circa 170 tossine, suddivise in 2 gruppi; in particolare, al gruppo A appartiene la tossina T-2, sintetizzata da alcune specie di funghi appartenenti al genere Fusarium; a seguito del suo rapido assorbimento a livello enterico, tale tossina produce una forte azione dermotossica, epatotossica, teratogena, embriotossica, emolitica ed emorragica, causando danni cellulari soprattutto a carico dei tessuti a rapido accrescimento, quali linfonodi e timo, del midollo osseo, della milza e dell’intestino; è responsabile della sindrome nota come aleukia (o leucopenia) tossica alimentare.
Molti prodotti alimentari consumati quotidianamente in ambiente domestico e/o extra-domestico si prestano alla diffusione volontaria di agenti biologici in funzione delle seguenti caratteristiche:
- la velocità delle fasi correlate all’immissione sul mercato da parte dei produttori, alla catena distributiva e alla disponibilità per un elevato numero di consumatori;
- la complessità, correlata al sistema di concatenamento delle aziende coinvolte nella catena, che complica i processi di rintracciabilità, al legame causa-effetto mai specifico, alla sintomatologia differita e/o aspecifica di molti patogeni, che ne consente una elevata diffusione prima della loro corretta identificazione, determinando, conseguentemente, un ritardato ritiro/richiamo del prodotto contaminato;
- l’opportunità, intesa quale aumento esponenziale dei pasti consumati fuori porta e del numero di potenziali utenti raggiungibili da uno stesso prodotto;
- la spettacolarità, considerato il forte impatto mediatico delle MTA, che toccano corde sensibili della psiche individuale e collettiva.
In relazione alla probabilità di un loro impiego quali strumento/veicolo di attacchi bioterroristici, è possibile attribuire ai vari alimenti una diversa classe di rischio, correlata alla capacità di essere inquinabili, alla condizione che l’agente inquinante permanga attivo fino al momento del consumo, alla capacità del lotto contaminato di raggiungere il più elevato numero di consumatori nel più breve tempo possibile, alla diffusione e penetrabilità del mercato, alla velocità di consumo e al legame tra i fattori consumo del prodotto, tradizione, epoca di consumo. Per quanto detto, gli alimenti possono essere suddivisi nelle classi:
- alto rischio, materie prime appartenenti a determinate categorie merceologiche, quali il latte di mungitura, gli alimenti liquidi, l’acqua erogata dagli acquedotti pubblici, le acque minerali e le bevande in generale, le conserve alimentari, il pane ed altri prodotti da forno, gli ovoprodotti; essi hanno in comune il fatto che da uno stesso lotto possono essere ricavate migliaia di confezioni e che la loro velocità distributiva è molto elevata;
- medio rischio, carni lavorate, prodotti a base di carne e insaccati, paste farcite ripiene, pasta e prodotti della pesca d’allevamento; la possibilità di frazionamento è inferiore alla precedente categoria;
- basso rischio, prodotti a medio-lunga stagionatura, uova, frutta, prodotti della pesca non allevati; la manomissione richiederebbe un notevole impegno, un grande dispendio di risorse e una oggettiva difficoltà di attuazione.
Vigilanza sui fornitori nazionali e certificazione sanitaria delle derrate alimentari destinate ai contingenti militari all’estero
In esito al percorso normativo, iniziato con il D. Lgs. n. 193/2007, proseguito con il Codice dell’Ordinamento Militare (D. Lgs. 66/2010 (31)) e giunto a maturazione con il D. Lgs. 27/2021 (32), il Ministero della Difesa, nella fattispecie l’Ispettorato Generale della Sanità Militare (IGESAN) e le relative Autorità Sanitarie Delegate di Forza Armata (33) (F.A.), è stato individuato quale Autorità Competente (AC) per le attività di Controllo Ufficiale (CU) e le Altre Attività Ufficiale (AAU), previste dal Reg. UE n. 625/2017, nelle strutture militari, estendendone l’ambito operativo agli stabilimenti esterni che forniscono merce alle FF.AA. stesse, previo coordinamento con le ASL arealmente competenti.
L’attività di vigilanza sui fornitori e sul servizio di preparazione e somministrazione di alimenti e bevande presso le imprese alimentari di competenza, viene effettuata ai sensi della normativa (comunitaria e nazionale) vigente, nonché in ottemperanza a direttive/circolari sia di natura Interforze, sia di singola F.A. (l’Autorità Sanitaria per l’Arma dei Carabinieri è costituita dal Dipartimento per l’Organizzazione Sanitaria e Veterinaria del Comando Generale dell’Arma dei Carabinieri, che si articola sul Servizio per la Sanità e il Servizio per la Veterinaria).
Le procedure di vigilanza si estrinsecano sulla base dei principi della legislazione alimentare (Reg. CE n. 178/2002), dell’igiene degli alimenti (Regg. CE n. 852/2004 e n. 853/2004), dei requisiti microbiologici (Reg. CE n. 2073/2005 e s.m.i.) e dell’obbligo di informazione ai consumatori (Reg. UE n. 1169/2011), con l’applicazione degli eventuali provvedimenti prescrittivi/sanzionatori, assunti quale AC, di rilevanza penale o amministrativa (art. 138 del Reg. UE n. 625/2017 e iter procedurale ex Legge n. 689/1981). Le modalità di effettuazione del CU sono quelle previste dall’art. 14 del cit. Reg. UE n. 625/2017 e, per la parte di specifico interesse, si concentrano sulla verifica del piano di autocontrollo aziendale degli OSA, redatto in aderenza al sistema HACCP (ex art. 5 del Reg. CE n. 852/2004), dei pre-requisiti e requisiti di struttura e di processo, nonchè della tracciabilità/rintracciabilità (ex art. 18 del Reg. CE n. 178/2002) e della qualità microbiologica delle materie prime e dei prodotti pronti al consumo. Per una maggiore efficacia delle predette attività, grazie a uno specifico Protocollo d’Intesa tra Ministero della Difesa e Ministero della Salute, ciascun Vertice Sanitario di F.A. ha ottenuto le credenziali di accesso, quale AC, sulla piattaforma on line (i-RASFF) del sistema RASFF, con la possibilità di creare e ricevere, per il tramite di IGESAN, le allerte inerenti ai prodotti alimentari entrati nel circuito della ristorazione collettiva militare.
Per quanto concerne l’esportazione delle derrate alimentari (e dei MOCA) destinate ai contingenti militari d’istanza nei TT.OO. esteri, l’apparato dei controlli e della loro conduzione viene specificamente regolamentato dalla Direttiva Interforze IGESAN - 003, che rafforza necessariamente il sistema di vigilanza, considerata la grande valenza strategica, per chi persegue finalità terroristiche, rappresentata dai reparti schierati a supporto di Missioni internazionali ad egida ONU/NATO/ EUFOR. Le operazioni vengono effettuate dall’AC incaricata (34), che presiede all’intera fase di carico delle derrate nel vano del mezzo di trasporto, al fine di verificare che non vengano introdotti colli non certificati e/o che non avvenga alcuna alterazione di quelli verificati nelle pregresse operazioni di controllo, e, al termine, appone il sigillo di chiusura del vano, che deve giungere inalterato fino a destinazione (35). Ad integrazione del controllo documentale, l’AC si avvale della possibilità di consultare il Sistema Informativo di Tracciabilità TRACES - NT, il cui accreditamento per le FF.AA. è frutto del suindicato Protocollo d’intesa tra il Ministero della Difesa e il Ministero della Salute.
Conclusione - Il futuro: Hazard Analysis and Risk-based Preventive Controls (HARPC)?
Come premesso, l’intero apparato normativo della UE in materia di igiene dei prodotti alimentari e delle correlate attività di CU è fondato sull’applicazione del sistema HACCP (36), che viene, pertanto, considerato l’unico strumento operativo efficace in termini di lotta alla minaccia bioterroristica. Le stesse FF.AA., seppure con le loro peculiarità, agiscono in tale contesto, nel quale, come analizzato, divengono essenziali la verifica e la vigilanza sulle procedure di autocontrollo poste in essere dagli Operatori del Settore Alimentare (OSA) appaltatori per i servizi indicati (gestione esternalizzata).
Negli USA, dal 15 settembre 2015, il metodo HACCP è stata oggetto di aggiornamento da parte della Food and Drug Administration (FDA), attraverso il c.d. Food Safety Modernization Act (FSMA), un pacchetto normativo che obbliga tutte le aziende che producono, manipolano, detengono e/o stoccano prodotti alimentari destinati al mercato statunitense ad adottare un Sistema di Gestione della Sicurezza Alimentare (37) (SGSA) in linea con quanto definito dal regolamento sui Preventive Controls for Human Food.
Per la materia trattata, sono di particolare interesse due rilevanti aspetti differenziali tra la nuova metodica, definita, per l’appunto, Hazard Analysis and Risk-based Preventive Controls (HARPC), e quella HACCP:
1. la tipologia di rischi presi in considerazione (Hazard Analysis), in quanto, mentre l’HACCP individua tre categorie di pericolo (biologico, chimico e fisico) da contaminazione accidentale naturale per la sicurezza alimentare, l’HARPC ne considera dodici, tra cui, in particolare, i pericoli introdotti intenzionalmente (azioni intenzionali di contaminazione e atti di bioterrorismo);
2. il concetto di controllo preventivo (Preventive Controls), nella considerazione che, mentre l’HACCP ha un approccio reattivo nei confronti di un pericolo (aspetta che accada per porvi rimedio), l’HARPC ha un approccio proattivo, cioè punta a prevenire i pericoli che si possono verificare in una fase iniziale, ivi compresa l’azione di natura bioterroristica.
Risulta evidente come l’HARPC costituisca l’evoluzione migliorativa dell’HACCP, quale metodica di riferimento per l’attuazione delle procedure di autocontrollo aziendale nel settore della sicurezza alimentare, puntando il focus sull’estensiva applicazione delle misure di c.d. Food Defense, funzionali all’individuazione dei nuovi agenti di rischio (sabotaggio, attacco bioterroristico) e all’adozione delle soluzioni atte a prevenire il verificarsi dei rischi analizzati (ad es. la sensibilizzazione dei quadri dirigenziali, le misure di videosorveglianza e di videoregistrazione delle aree di stoccaggio delle derrate, l’applicazione di dispositivi anti-intrusione con allarme automatico presso gli accessi dello stabilimento, etc.).
L’autore ritiene auspicabile, dunque, che, come già avvenuto per l’HACCP (metodo elaborato negli USA, negli anni Sessanta del secolo scorso, e finalizzato a garantire la sicurezza dei pasti destinati agli astronauti della NASA), la UE prenda spunto dalla FDA per implementare la metodica dell’autocontrollo e adottare il sistema HARPC, quale strumento evoluto e proattivo di prevenzione nei confronti degli atti di bioterrorismo alimentare; l’auspicio e la speranza, infatti, sono quelli di non andare incontro a ulteriori trenta anni di attesa (38) (tanti ce ne sono voluti nel caso dell’HACCP) prima di abbracciare questa nuova metodica, che fonda le proprie radici nella imprescindibile tutela del consumatore e che, pertanto, possiede nel suo patrimonio genetico l’essenza stessa della food safety.
______________________________________________________________________
1) Reperiti in natura o modificati per lo scopo, al fine di aumentarne l’effetto patogeno, la virulenza e/o la contagiosità. (2) “In materia di tutela della salute e della sicurezza nei luoghi di lavoro”. (3) Ai quattro gruppi di rischio corrispondono i quattro livelli di biosicurezza in laboratorio (Biosafety Level, BSL 1-4; fonte WHO, CDC). (4) Nel gruppo 4 vengono collocati Filoviridae (Ebola, Marburg), CCHF-V, Lassavirus e Variolavirus. (5) In termini di disponibilità di terapie efficaci o di misure di profilassi attiva e/o passiva. (6) A questa classificazione fa riferimento anche il Ministero della Salute - DG Prevenzione Sanitaria, che assegna a queste categorie priorità alta (“A”), media (“B”) e bassa (“C”). (7) Gli agenti biologici di categoria «A» sono: Variola majoir (virus del vaiolo), Bacillus anthracis, Yersinia pestis, tossina botulinica di Clostridium botulinum, Francisella tularensis, virus delle febbri emorragiche, Filoviridae (Ebola, Marburg), Arenavirus (febbre di Lassa, Machupo), Bunyaviridae (CCHF) e Flaviviridae (febbre gialla). (8) In categoria «B» sono collocati Alphavirus (agente di encefaliti virali), Coxiella burnetii (agente della «Febbre Q»), Brucella spp., tossina epsilon di Clostridium perfringens, enterotossina tipo B di Staphilococcus aureus, minacce alla sicurezza degli alimenti (Salmonella spp., Shigella spp., E.coli O157:H7), minacce alla sicurezza dell’acqua (Vibrio cholerae e Cryptosporidium parvum), Burkholderia mallei (morva) e pseudomallei, Chlamydia psittaci, Rickettsia prowazekii (febbre tifoide), tossina ricina da Ricinus communis (origine vegetale). (9) In categoria «C», sono collocati patogeni emergenti, quali Nipahvirus, Hantavirus, Coronavirus e virus influenzali in grado di causare pandemia. (10) La successiva circolazione marittima della malattia (i ratti presenti a bordo delle navi costituirono il serbatoio dell’agente eziologico) causò il rapido diffondersi della pandemia, la c.d. Peste Nera, che causò in Europa il decesso di circa il 30% della popolazione dell’epoca (tra 20 e 25 milioni di morti) nel periodo 1348-1353. (11) 22 casi accertati di intossicazione (11 per via inalatoria), di cui 5 mortali; il 4 aprile 2005 emerse il nome di Bruce E. Ivins come principale indiziato dell’atto terroristico. (12) Generalmente artropodi. (13) Rappresenta il rapporto percentuale tra il numero dei decessi e il numero dei soggetti malati (gli agenti letali sono quelli in grado di causare la morte in almeno il 10% dei casi non sottoposti a cura). (14) Sostanze chimiche prodotte da organismi viventi. (15) Alternativamente, in funzione del tropismo, si possono suddividere in citotossine, enterotossine e neurotossine, (quelle stafilococciche, che agiscono direttamente sul centro encefalico del vomito, e le tossine botuliniche, che agiscono sulle terminazioni nervose della placca neuro-motrice, causando paralisi muscolare flaccida). (16) Rappresenta la quantità di tossina necessaria a causare la morte del 50% degli individui esposti e non protetti. (17) Gli obiettivi tattici prediligono necessariamente l’impiego di tossine. (18) Potenziali candidati: virus dell’Influenza Aviaria A (H5:N1), Coronavirus, Pandoravirus, il protista Naegleria fowleri, la tossina H del Clostridium botulinum. (19) Regg. CE n. 178/2002, n. 852/2004, n. 853/2004 e Reg. UE n. 625/2017. (20) Hazard Analysis and Risk-based Preventive Controls. (21) Ne sono noti 7 tipi antigenici (A, B, C, D, E, F, G). (22) Destinati al consumo diretto, senza ulteriori trattamenti termici. (23) Per enterite necrotizzante. (24) In particolare, carni crude o poco cotte (per es. hamburger cotti rapidamente, senza raggiungimento a core della temperatura di inattivazione delle forme vitali del batterio) e latte non pastorizzato somministrato senza previa bollitura. (25) Shigellosi o dissenteria bacillare, caratterizzata dalla bassa dose infettante (10-200 ufc/g). (26) Conseguenza dell’intensa disidratazione causata dalla sintomatologia gastroenterica. (27) Un individuo adulto può arrivare a eliminare 20 l di liquidi in 24 ore. (28) L’inattivazione delle oocisti avviene mediante un trattamento di congelamento o di pastorizzazione. (29) Per il consumo di molluschi bivalvi contaminati; nei casi estremi può subentrare la paralisi, il coma e la morte. (30) Dove si concentra, in particolar modo, a livello di gonadi, fegato, intestino e pelle. (31) Art. 182 e ss. (32) Art. 2, comma 8. (33) Per l’Arma dei Carabinieri, il Dipartimento per l’Organizzazione Sanitaria e Veterinaria del Comando Generale dell’Arma dei Carabinieri, articolato sul Servizio per la Sanità e il Servizio per la Veterinaria. (34) Un Ufficiale veterinario, opportunamente formato, mediante training di F.A., e attestato quale certificatore (attribuzione di codice alfa-numerico univoco di riconoscimento). (35) Nel caso in cui l’Autorità Doganale proceda alla rottura del sigillo per eventuali attività di verifica, dovrà, successivamente, apporne uno nuovo, integro, accompagnato dalla relativa dichiarazione. (36) Il metodo, che si articola sui due momenti fondamentali della valutazione del rischio e dell’individuazione delle misure per il controllo dei pericoli, è subordinato alla presenza dei c.d. pre-requisiti e si articola sui sette principi elaborati dal Codex Alimentarius (1993). (37) Vedasi sull’argomento la norma UNI EN ISO 22000:2018. (38) Direttiva 93/43/CEE; D. Lgs. n. 155/1997, attuazione nazionale. Bibliografia AGARWAL, R. et al. (2004). Biological Warfare - An Emerging Threat. Journal of the Association of Physicians of India, 52: 733-738. AMBRUS, J.L. et al. (2007). Bioterror, agroterror, and new diseases. Discov Med, 7 (38): 82-87. AURELI, P. (2002). Uso bellico e terroristico della tossina botulinica. Not Ist Super Sanità, 15 (6): 17-18. AUSTRALIA GROUP (2018). Common Control List Handbook. Volume II: Biological Weapons-Related Common Control Lists. United States Government. BELLUZZI, G. et al. (2005). Il bioterrorismo. Le aziende di produzione e di trasformazione: prevenzione e gestione delle crisi. Parte III. Large An Rew, 11 (4): 35-44. CENCIARELLI, O. (2013). Biological Weapons and Bio-Terrorism: a Review of History and Biologi-cal Agents. Defence S&T Tech Bull, 6 (2): 111-129. COMANDO DELLE FORZE OPERATIVE TERRESTRI (2010). N. 6295 Aggressivi biologici. COLAVITA G., (2023). Igiene e Tecnologie degli Alimenti. Milano: Point Veterinaire Italie Srl. COMMISSIONE DELLE COMUNITÀ EUROPEE (2003). Comunicazione della Commissione al Consiglio e al Parlamento Europeo sulla Cooperazione nell’Unione Europea in materia di predisposizione e reazione agli attentati biologici e chimici (Sicurezza Sanitaria). CRIVELLARO, M. (2004). La gestione dei rischi di sabotaggio alimentare. Thiene (VI): CSQA Certificazioni. DA SILVA, E.J. (1999). Biological warfare, bioterrorism, biodefence and the biological and toxin weapons convention. Electronic Journal of Biotechnology. 2 (3): 99-129. GEISSLER, E. (2004). Biological and toxin weapons research, development and use from middle ages to 1945. Oxford: Oxford University Press. GOPALAKRISHNAKONE, P. (2015). Biological Toxins and Bioterrorism. Dordrecht (NL): Springer Science+Business Media. GOPALAKRISHNAKONE, P. (2016). Marine and Freshwater Toxins. Dordrecht (NL): Springer Science+Business Media. JANSEN, H. J. et al. (2014). Biological warfare, bioterrorism, and biocrime. Clin Microbiol Infect, 20 (6): 488-496. MADSEN, J.M. (2003). Agenti Biologici come armi. Roma: Manuali MSD. MARTY, A.M. (2001). History of the development and use of biological weapons. Clin Lab Med, 21: 421-434. MINISTERO DELLA SALUTE - Direzione Generale della Prevenzione. Agenti biologici categoria A (Alta Priorità). MINISTERO DELLA SALUTE- Piano di Formazione USMAF (2018). Classificazione degli agenti infettivi in relazione alla sicurezza biologica. NASSO, M. e ROMOLO F.S. (2007). La microbiologia forense e il pericolo del bioterrorismo. Emergency Care Journal, II, 1: 30-36. NATO STANDARD (2010). ATP-3.8.1 Volume I - CBRN Defence on Operations. Nato Standardization Office (NSO). NATO STANDARD (2016). ATP-45 Warning and reporting and hazard prediction of chemical, biological, radiological and nuclear incidents (operators manual). Nato Standardization Office (NSO). NATO STANDARD (2019). AMedP-4.12 Food and Water Defence. Nato Standardization Office (NSO). NATO STANDARD (2022). AMedP-4.14 Food and Water Safety, Defence and Production in NATO Naval Operations. Nato Standardization Office (NSO). STATO MAGGIORE DELLA DIFESA - Ispettorato Generale della Sanità Militare (2014). SMD-IGESAN 003 Direttiva interforze inerente alla attività di controllo igienico-sanitario delle derrate alimentari ed alla sicurezza degli alimenti per i contingenti impiegati all’estero. STATO MAGGIORE DELLA DIFESA e ISPETTORATO GENERALE DELLA SANITÀ MILITARE (2017). SMD-IGESAN 005 Direttiva interforze per la prevenzione dell’importazione di organismi responsabili di epizoozie e zoonosi. SZINICZ, L. (2005). History of chemical and biological warfere agents. Toxicology, 214: 167-181. TOROK, T. J. et al. (1997). A large community outbreak of salmonellosis caused by intentional conta-mination of restaurant salad bars. JAMA, 278 (5): 389-395. TREVISANATO, S. I. (2007). The “Hittite plague”, an epidemic of tularemia and the first record of biological warfare. Med Hypotheses, 69 (6): 1371-1374. TROIANO, G. (2016). Guerra batteriologica e bioterrorismo: ancora una sfida per la sanità pubblica. Working Paper of Public Health, 1: 1-10. UK, US E SOVIET GOVERNMENTS (1972). Convention on the Prohibition of the Development, Pro-duction and Stockpiling of Bacteriological (Biological) and Toxin Weapons and on Their Destruction. VAN AKEN, J. e HAMMOND, E. (2003). Genetic engineering and biological weapons. EMBO Rep., 4 (Suppl 1): S57-S60. WARHEIT, D.B. (2004). Biological agents with potential for misuse: a historical perspective and defensive measures. Toxicolgy and Appl Pharmac, 199: 71-84.